I tensioattivi anionici ,componenti fondamentali dei detergenti, sono composti organici sintetici ad eccezione del sapone caratterizzati dalla presenza nella molecola di due gruppi, uno idrofobo e uno idrofilo; poiché in genere un tensioattivo è usato in soluzione acquosa, la parte idrofila rappresenta il gruppo solubilizzante.
La parte idrofoba della molecola è rappresentata da una catena idrocarburica, talvolta alogenata, con lunghezza media da dieci a venti atomi di carbonio, che è simboleggiata con R. La parte idrofila solubilizzante è di natura diversa e in base ad essa si fa una classificazione primaria dei tensioattivi: si distinguono così quattro classi: anionici, non ionici, cationici, anfolitici.
Struttura
La struttura generale di un tensioattivo può essere visualizzata in figura:
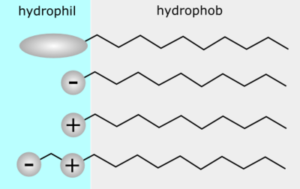 A causa della contemporanea presenza nella molecola di un tensioattivo di una parte idrofoba e di una parte idrofila si ha una modificazione di alcune proprietà chimico-fisiche delle soluzioni acquose, anche diluite, di tali composti. In particolare essi agiscono sulle interfacce liquido-gas, liquido-liquido e liquido-solido. Da queste proprietà deriva appunto il nome di tensioattivi. I tensioattivi sono classificati in quattro classi caratterizzate dal tipo di gruppo idrofilo solubilizzante, e in diverse sottoclassi che raggruppano i diversi tipi chimicamente affini nell’ambito di una classe.
A causa della contemporanea presenza nella molecola di un tensioattivo di una parte idrofoba e di una parte idrofila si ha una modificazione di alcune proprietà chimico-fisiche delle soluzioni acquose, anche diluite, di tali composti. In particolare essi agiscono sulle interfacce liquido-gas, liquido-liquido e liquido-solido. Da queste proprietà deriva appunto il nome di tensioattivi. I tensioattivi sono classificati in quattro classi caratterizzate dal tipo di gruppo idrofilo solubilizzante, e in diverse sottoclassi che raggruppano i diversi tipi chimicamente affini nell’ambito di una classe.
Classificazione
Le quattro classi sono descritte di seguito in ordine di importanza :
1) Anionici : carbossilati, solfonati, solfati, vari
2) Non ionici : etossilati eterei, etossilati esterei, etossilati ammidici, etossilati amminici
3) Cationici : ammine, ammonio quaternario, altri derivati dell’azoto, vari
4) Anfolitici
Tensioattivi anionici
La parte idrofila solubilizzante dei tensioattivi anionici è costituita da un gruppo polare che risulta carico negativamente in soluzione acquosa. I gruppi più importanti di queste classi sono: -COO–,
-SO3–, -OSO3–. Il gruppo solfato è il solubilizzante più forte, il gruppo carbossilato è il più debole e in soluzioni non alcaline o in presenza di cationi polivalenti porta addirittura prodotti insolubili.
Carbossilati
I sali alcalini di acidi carbossilici (saponi) sono i tensioattivi più vecchi, meglio conosciuti e più importanti. Hanno origine naturale: per saponificazione dei grassi e oli naturali si ottengono acidi lineari, ramificati, insaturi, idrossisostituiti, ecc. I più usati come saponi sono gli acidi lineari con formula generale R-COOH con R costituito da dieci a ventidue atomi di carbonio. In genere si usano sali di sodio e di potassio.
Solfonati
In questa classe di tensioattivi il gruppo idrofilo –SO3– è legato alla catena idrocarburica mediante un legame C-S. il gruppo idrofilo è un acido forte che non tende a idrolizzare come nel caso di –COO– e che mostra rispetto a questo un maggior potere solubilizzante. Inoltre il legame C-S è molto stabile e pertanto i solfonati non presentano problemi durante l’impiego nelle più svariate condizioni di pH.
Alchilarilsolfonati
A questa classe appartengono i tensioattivi sintetici più diffusi attualmente, cioè gli alchilbenzensolfonati. I nuclei aromatici più diffusi sono benzene e naftalene, mentre le catene alchiliche più usate sono intorno a C6-C8 nel caso della naftalene e C11-C13 nel caso del benzene.
Alcansolfonati in cui il gruppo idrofilo –SO3– è distribuito in modo statistico lungo la catena idrocarburica.
Solfati
Il gruppo idrofilo di questa classe di tensioattivi –OSO3– è quello, tra i gruppi anionici esaminati, presenta il maggior potere solubilizzante.
Poiché nei solfati è presente un legame C-O-S che ha una certa tendenza all’idrolisi, questi prodotti non possono essere impiegati in condizioni di pH molto spinte, specie per valori di pH acido. Per quanto riguarda la parte idrofoba della molecola essa può essere di diversa natura. Si possono fare comunque due grosse distinzioni: prodotti di origine naturale e prodotti di sintesi messi a punto dall’industria petrolchimica.
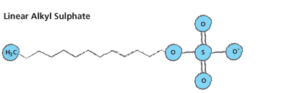 Alchilsolfati
Alchilsolfati
I prodotti del campo C12-C18 sono tipici tensioattivi usati per la preparazione dei detergenti sintetici fin dagli anni ’30 negli Stati Uniti. Gli alchilsolfati si possono preparare secondo due reazioni generali che prevedono rispettivamente l’impiego di alcoli primari e di olefine come materie prime:
R-OH + H2SO4 → R-OSO3H + H2O
R-CH=CH-R’ + H2SO4 → R-CH2CH(OSO3H)-R’
La differenza fondamentale fra le due reazioni è che con la prima si ottengono solfati di alcoli primari, mentre con la seconda si ottengono solfati di alcoli secondari. I solfati primari sono caratterizzati da alto potere schiumogeno, imbibente, detergente, emulsionante e disperdente e trovano impiego per la preparazione di detergenti sintetici solidi e in cosmetica.
Etossisolfati
Allo scopo di aumentare la solubilità degli alchilsolfati, specie in prodotti liquidi, si usano etossisolfati. Questi derivano dalla combinazione della tecnica dell’etossilazione e della successiva solfatazione; in tal modo con l’introduzione in genere di 2-4 molecole di ossido di etilene si accresce il contenuto della parte idrofila della molecola. Si hanno due tipi fondamentali di etossisolfati: derivati dagli alchilfenoli e dagli alcoli.
I primi prodotti sono stati largamente usati in passato, ma a partire dagli anni ’60 si è avuto un loro progressivo declino a vantaggio dei secondi a causa della maggiore disponibilità degli alcoli di sintesi e maggiore biodegradabilità dei derivati di questi ultimi.
Solfati vari
Sono caratterizzati dalla presenza di altri gruppi oltre a quello di –OSO3–. Gli oli solfatati sono ottenuti a partire da oli e grassi naturali che chimicamente sono gliceridi di acidi grassi in parte insaturi o idrossilati. Gli oli solfonati sono stati preparati a partire dal 1850; hanno trovato applicazione come agenti emulsionanti e bagnanti e come adiuvanti della tintura nell’industria tessile, applicazioni tuttora in uso.
Anionici vari
In questa classe vi sono alcuni tipi di tensioattivi come gli ossiacidi del fosforo e i derivati della lignina.
Derivati del fosforo
Il gruppo anionico contenente fosforo può essere considerato un altro gruppo solubilizzante e I tensioattivi che ne derivano sono di due tipi fondamentali: esteri dell’acido fosforico nei quali è presente il legame C-O-P, e acidi fosfonici, nei quali è presente il legame C-P. I primi sono conosciuti come prodotti con elevata tensioattività, ma bassa resistenza agli acidi e agli ioni calcio, che provocano formazione di prodotti insolubili.
