Il solfuro di carbonile fu descritto nel 1841 e caratterizzato nel 1867. Il solfuro di carbonile è la specie dello zolfo più stabile e presente in natura e viene prodotto nelle acque superficiali mediante fotolisi di composti organici dello zolfo disciolti.
Esso è una sostanza infiammabile e può formare miscele esplosive con l’aria. Ha azione corrosiva per i metalli comuni in presenza di umidità e reagisce vigorosamente con gli ossidanti.

Il solfuro di carbonile è detto anche ossisolfuro di carbonio presenta una struttura lineare simile a quella del biossido di carbonio. Nella molecola infatti il carbonio è ibridato sp e si lega tramite doppio legame sia all’ossigeno che allo zolfo
L’unica differenza risiede nelle lunghezze di legame. Nel biossido di carbonio la lunghezza di legame carbonio-ossigeno è di 116.3 pm mentre nel solfuro di carbonile la lunghezza di legame carbonio-ossigeno è di 115.78 pm mentre quella carbonio-zolfo è di 156.01 pm.
Proprietà del solfuro di carbonile
Il solfuro di carbonile è un gas inodore e scarsamente solubile in acqua contenente zolfo. È il principale gas contenete zolfo presente nell’atmosfera dove ha un lungo tempo di permanenza di circa 4 anni. A causa della sua relativa inerzia si diffonde nella stratosfera dove si ossida in particelle di solfato e contribuisce alle reazioni che coinvolgono la chimica dell’ozono stratosferico.
A differenza del dimetilsolfossido che è ossidato fotochimicamente nella troposfera è assorbito dalle piante dove si idrolizza in biossido di carbonio e solfuro di idrogeno tramite azione enzimatica.
Viene prodotto negli oceani dall’ossidazione fotochimica dei composti organici solforati pertanto è un importante composto che entra nel ciclo dello zolfo e fa parte dei gas prodotti da un’eruzione vulcanica.
Sintesi
Fu sintetizzato a partire da tiocianato di potassio e acido solforico ad una temperatura di 40-50 °C secondo la reazione:
KSCN + 2 H2SO4 + H2O → KHSO4 + NH4HSO4 + COS
da cui si ottiene, oltre al solfuro di carbonile, anche il solfato acido di potassio e di ammonio
A livello industriale può essere ottenuto dalla reazione tra monossido di carbonio e zolfo a circa 800°C:
CO + S → COS
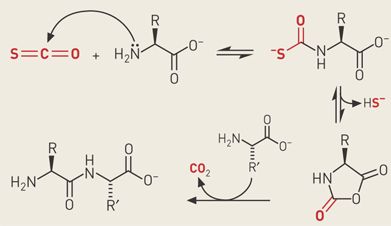
Reazione con gli amminoacidi
Vari studi scientifici hanno dimostrato che esso reagisce con gli amminoacidi in soluzione acquosa per dare peptidi
Potrebbe quindi avere giocato un ruolo fondamentale nell’evoluzione prebiotica