Le reazioni di addizione, si verificano su substrati che possiedono legami π e, per questo motivo, le reazione di addizioni sono caratteristiche di sistemi contenenti legami multipli.
Nelle reazioni di addizione nucleofila il reattivo, entità ricca di elettroni, costringe gli elettroni π del legame multiplo a localizzarsi su uno dei due atomi, con formazione di un anione, il quale, poi, assume una entità positiva E+ (generalmente H+ o M+) presente nel sistema.
I substrati che danno reazione di addizione nucleofila presentano atomi di carbonio ibridati sp2 e sp in cui vi sia una polarizzazione degli elettroni π per effetto induttivo e mesomero e possono essere riuniti in due gruppi:
- Composti carbonilici ed eterocarbonilici
- Composti con legami multipli attivati
Reattività
La reattività è influenzata dagli effetti induttivi del sostituenti in α al legame multiplo. L’impiego di solventi polari aprotici, che aumentano la forza dei nucleofili anionici solvatando l’entità elettrofila ad essi associata, favorisce le reazioni di addizione nucleofila.
Quest’ultima, pur richiedendo normalmente una catalisi basica, può essere favorita, nel caso di composti carbonilici o etero analoghi, da una debole catalisi acida. In generale nella reazione di addizione nucleofila, si ha un passaggio da un carbonio ibridato sp2 planare a sp3 tetraedrico.
Il nucleofilo, durante la reazione, si avvicina al carbonio nel piano degli elettroni π (perpendicolare al piano della molecola) e, data la polarità del substrato, l’attacco può avvenire sia sopra che sotto il piano molecolare. Quando non è presente nella molecola nessun centro di asimmetria, l’addizione è ugualmente probabile da ambo i lati: si ottiene, così una miscela racemica, anche se l’attacco antiparallelo che conduce a una forma alternata è più probabile di un attacco parallelo, da cui si ottiene la forma eclissata meno stabile.
Quando, invece, vicino all’atomo di carbonio ibridato sp2 è presente un centro di asimmetria, la formazione di un secondo centro di asimmetria per l’addizione nucleofila è influenzata dalla conformazione del centro preesistente. Questo comporta la formazione di un solo diastereoisomero per cui la reazione è stereoselettiva e il centro di asimmetria preesistente produce un’induzione asimmetrica.
Tale stereo selettività viene spiegata con la regola di Cram-Felkin: lo stato di transizione più favorevole (più vicino al prodotto di partenza) è quello che deriva da un attacco antiparallelo nella conformazione in cui sono minime le interazioni tra i sostituenti presenti nella molecola”.
Meccanismo
Nella reazione di sostituzione nucleofila intervengono tre fattori fondamentali:
1) Formazione di un nuovo legame σ tra il nucleofilo Nu e il carbonio carbonilico
2) Rottura del legame π con formazione di un intermedio alcossido
3) Protonazione dell’intermedio alcossido con ottenimento di un derivato alcolico.
In funzione della reattività del nucleofilo, vi sono due possibilità:
- Forti nucleofili (anionici) si addizionano direttamente al carbonio carbonilico per dare un intermedio alcossido. Gli alcossidi vengono protonati con acido diluito:
Nu– + C=O → Nu-C-O–→Nu-C-OH. Esempi di tali nucleofili sono RMgX, RLi, LiAlH4 , NaBH4
- Nucleofili più deboli (neutri) necessitano che il gruppo C=O sia preventivamente attivato prima del loro attacco. Ciò può essere realizzato usando un acido in qualità di catalizzatore che protona l’ossigeno rendendo il sistema più elettrofilo:
C=O + H+ ⇌ CO+H
CO+H + Nu-H → HNu+-C-OH
HNu+-C-OH + :B ⇌ Nu-C-OH + HB
Esempi di tali nucleofili sono H2O, ROH, RNH2
Esempio
Un esempio di sostituzione nucleofila è costituito dalla reazione tra un alogenuro acilico e un nucleofilo: il gruppo carbonilico presenta una polarizzazione con una parziale carica positiva sul carbonio e una parziale carica negativa sull’ossigeno; d’altra parte, stante la maggior elettronegatività del cloro rispetto al carbonio, anche il cloro ha una parziale carica negativa.
Il nucleofilo attacca il carbonio carbonilico secondo il seguente schema:
successivamente si riforma il doppio legame carbonio ossigeno e si distacca dalla molecola lo ione cloruro:
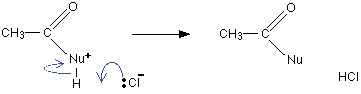
infine, lo ione cloruro prende l’idrogeno come ione H+ per dare il prodotto finale con formazione di HCl: