L’ ozonolisi del benzene dà, come prodotti di reazione il gliossale che è la più semplice delle dialdeidi e ha formula OCHCHO e il perossido di idrogeno.
In generale l’ozonolisi, detta scissione ossidativa, è una reazione in cui si verifica la scissione di un legame insaturo in un composto a seguito della reazione con l’ozono.
Pertanto è una reazione prevalentemente utilizzata per gli alcheni che comporta la rottura sia del legame σ che del legame π presenti nel doppio legame con formazione di due gruppi carbonilici.
Rispetto alle altre reazioni degli alcheni che portano alla rottura del doppio legame lasciando intatto lo scheletro carbonioso, questa reazione provoca la rottura del doppio carbonio-carbonio con formazione di due frammenti contenenti il gruppo carbonile.
A seconda del numero di gruppi R legati al doppio legame la scissione ossidativa porta alla formazione di aldeidi e/o chetoni.
Meccanismo dell’ozonolisi del benzene
L’ozonolisi del benzene avviene in due stadi.
Il primo stadio consiste nell’addizione elettrofila dell’ozono con formazione di un ciclo instabile detto triozonuro.
Esso è ottenuto dall’addizione di una molecola di ozono a ciascun legame π del benzene.
Pertanto ogni legame π è sostituito da due legami carbonio-ossigeno e il prodotto contiene, al posto di un doppio legame, due atomi di ossigeno atomi legati all’esterno dell’anello tra i 2 atomi di carbonio e un atomo di ossigeno all’interno dell’anello tra gli atomi di carbonio.
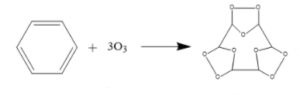
Nel secondo stadio il triozonuro è trattato con un agente riducente come zinco metallico e acqua.
L’intermedio si rompe dove è presente un legame carbonio-ossigeno-carbonio e l’ossigeno si combina con l’acqua per dare perossido di idrogeno. Si ottengono tre frammenti costituiti da molecole contenenti due atomi di carbonio legati tramite doppio legame all’ossigeno
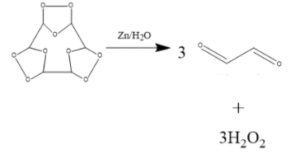
La molecola che si ottiene è il gliossale
Gliossale
Il gliossale è la più semplice delle dialdeidi e, a causa della sua bassa tossicità, è spesso utilizzato al posto della formaldeide.
È un composto di interesse industriale per la sintesi dell’imidazolo.
Inoltre è utilizzato come solubilizzante e agente reticolante nella chimica dei polimeri e per l’ottenimento di resine epossidiche di cui migliora la stabilità. È usato per reticolare formulazioni a base di amido nelle finiture tessili e nella carta
