Il dimetilsolfossido (DMSO) ha formula CH3SOCH3 ed è un composto organico appartenente alla famiglia dei solfossidi ovvero a quei composti in cui è presente un gruppo solfenile > S=O.
Stante l’elevata differenza di elettronegatività tra lo zolfo e l’ossigeno il legame si presenta polare e pertanto un solfossido può essere rappresentato dalle seguenti strutture limite di risonanza:
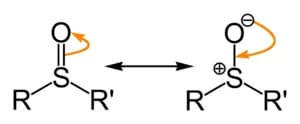
Il dimetilsolfossido è classificato come un solvente polare aprotico che si differenzia dai solventi polari protici come acqua, etanolo e acidi carbossilici in quanto non è un donatore di ioni H+.
Ha un elevato punto di ebollizione ed è miscibile con l’acqua e molti solventi organici come eteri, esteri, alcoli e composti aromatici ed è stabile a una temperatura superiore ai 100°C sia in ambiente acido che basico.
Il dimetilsolfossido ha assunto un ruolo importante negli ultimi anni in quanto alle ottime capacità solventi di composti sia organici che inorganici è economico e facilmente sintetizzabile. E’ un solvente di molti composti aromatici e idrocarburi insaturi, composti organici contenenti azoto o zolfo e di molti sali inorganici
Sintesi
Fu scoperto per la prima volta alla fine del XIX secolo come sottoprodotto del processo Kraft per produrre carta dalla pasta di legno e sintetizzato per la prima volta nel 1866 dal chimico russo Alexander Zaytsev. A livello industriale il dimetilsolfossido viene ottenuto per reazione del dimetilsolfuro e un eccesso di ossigeno alla temperatura di 15-50°C in presenza di NO2.
Può essere ottenuto dalla reazione tra il dimetilsolfuro e un perossido come H2O2 o un perossiacido.
Reazioni del dimetilsolfossido
Il dimetilsolfossido reagisce con forti agenti ossidanti per dare il dimetilsolfone CH3SOOCH3 ma in ambiente alcalino per NaClO l’ossidazione è accompagnata dalla clorazione per sostituzione dell’idrogeno con il cloro.
Il dimetilsolfossido può essere ridotto in presenza di forti agenti riducenti quali l’idruro di alluminio. I mercaptani riducono il dimetilsolfossido in ambiente acido per dare un tioetere e un disolfuro:
CH3SOCH3 + 2 RSH → CH3SCH3 + RSSR + H2O
Il dimetilsolfossido reagisce con gli idruri per dare un carbanione:
CH3SOCH3 + NaH → Na++ –CH2SOCH3 + H2
Quest’ultimo reagisce con gli alogenuri alchilici primari per dare un solfossido:
CH3(CH2)3CH2Br + –CH2SOCH3 → CH3(CH2)3CH2CH2SOCH3 + Br–
Il dimetilsolfossido può essere alogenato con cloro o bromo in ambiente basico.
La reazione tra DMSO, piridina e bromo in cloroformio a 0°C dà luogo alla formazione di bromometil, metil solfossido CH3SOCH2Br.
Il dimetilsolfossido è usato in molti processi industriali come, ad esempio:
- nella produzione di poliacrilonitrile
- l’estrazione di idrocarburi aromatici
- la fabbricazione di pesticidi e di prodotti usati dall’industria per la sverniciatura e per la pulizia.
