La deidroalogenzazione è una reazione in cui, a caldo, in presenza di una base forte come KOH in solvente alcolico, un alogenuro alchilico dà un alchene.
Un esempio di deidroalogenzazione è costituito dalla reazione tra bromoetano e KOH:
CH3CH2Br + KOH → CH2=CH2 + KBr + H2O
La reazione può avvenire anche in presenza di un alcossido piuttosto che di una base.
Meccanismo della deidroalogenazione
Il meccanismo della deidroalogenazione prevede la rimozione di un idrogeno sul carbonio in β, la formazione del doppio legame e la fuoriuscita dell’alogenuro.
La reazione di deidroalogenazione è una reazione di eliminazione e può quindi avvenite mediante meccanismo E2 o E1.
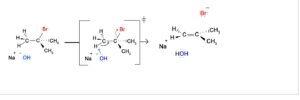
Nel caso il cui avvenga secondo un meccanismo E2 la reazione avviene in modo concertato con formazione di uno stato di transizione in cui vi è una parziale formazione del legame tra la base e l’idrogeno, la parziale formazione del doppio legame e la parziale rottura del legame carbonio-alogeno
La reazione può avvenire anche con meccanismo E1 quando l’allontanamento dell’alogeno dà luogo alla formazione di un carbocatione stabile. Ad esempio dal 2-cloro,2-metil propano si ottiene, nel primo stadio della reazione, un carbocatione terziario stabile: (CH3)3C-Cl → (CH3)3+ + Cl–. Nel secondo stadio della reazione la base attacca l’idrogeno in β e si forma il doppio legame
Fattori che determinano il meccanismo
I fattori che determinano quali dei due meccanismi ha luogo nella deidroalogenazione sono il tipo di:
- base: basi forti favoriscono il meccanismo E2 mentre basi deboli quello E1
- solvente: solventi polari protici stabilizzano il carbocatione e quindi favoriscono il meccanismo E1
- alogenuro alchilico: gli alogenuri alchilici primari danno luogo al meccanismo E2 stante la scarsa stabilità del carbocatione
Quando la reazione avviene tramite meccanismo E1 bisogna tener conto che il carbocatione può riarrangiarsi quindi si ottiene più di un prodotto di reazione.
In entrambi i casi le reazioni di sostituzione competono con quelle di eliminazione.
Nel caso in cui il meccanismo avvenga in modo concertato si può ottenere sia l’alchene che il prodotto di sostituzione.
Nel caso di alogenuri alchilici primari se la base è di piccole dimensioni il meccanismo SN2 compete fortemente con quello E1 infatti il suo avvicinamento al carbonio non è impedito.
Ad esempio facendo reagire il bromoetano con l’etossido di sodio in presenza di alcol a 55°C si forma in ragione del 10% il prodotto di eliminazione ovvero l’etene e in ragione del 90% il prodotto di sostituzione ovvero il dietiletere.
CH3CH2O– + CH3CH2Br → CH3CH2OCH2CH3 (SN2 90%)
CH3CH2O– + CH3CH2Br → CH2=CH2 (E2 10%)
Nel caso di alogenuri alchilici secondari il carbonio è più impedito e prevale il meccanismo E2 così come avviene nel caso di alogenuri alchilici terziari in cui se la reazione avviene ad alte temperature
Se si possono formare due alcheni a seguito della deidroalogenazione di un alogenuro alchilico si forma quello più sostituito. Ad esempio il principale prodotto della reazione del 2-bromobutano è il 2-butene piuttosto che l’1-butene