I metallo carbonili sono complessi costituiti da metalli di transizione e da leganti di monossido di carbonio. Tali complessi sono usati nelle sintesi organiche quali catalizzatori e quali precursori di altri complessi organometallici.
Il monossido di carbonio è formato da un atomo di carbonio legato a un atomo di ossigeno tramite un triplo legame che è costituito da due legami covalenti e da un legame dativo.
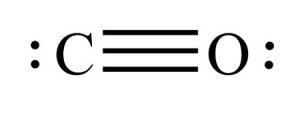
Il monossido di carbonio è un legante di tipo L ovvero è un legante neutro che ha 2 elettroni e si lega ai metalli di transizione tramite una retrodonazione π . In tale tipo di legame il metallo mette a disposizione elettroni per riempire gli orbitali antileganti π* di CO con la formazione di un legame complessivo dato da una combinazione di donazione di elettroni da parte di una base di Lewis a cui fa seguito une retrodonazione elettronica da parte della specie che funge da acido di Lewis.
Il monossido di carbonio è un forte donatore di elettroni σ e un buon accettore di elettroni π. Le proprietà elettroniche del metallo influenzano il peso della retrodonazione nei metallo carbonili.
Caratterizzazione
La tecnica più importante per la caratterizzazione dei metallo carbonili è la Spettroscopia I.R.: la frequenza corrispondente allo stretching Carbonio-Ossigeno corrisponde a 2143 cm-1 per il monossido di carbonio gassoso. I metallo carbonili presentano tutti, a causa della retrodonazione, frequenza più basse:
|
Complesso |
Frequenza (cm-1) |
|
V(CO)6 |
1976 |
|
Cr(CO)6 |
2000 |
|
Mn2(CO)10 |
2013 |
|
Fe(CO)5 |
2023 |
|
Co2(CO)8 |
2044 |
|
Ni(CO)4 |
2057 |
|
[Ti(CO)6]2- |
1747 |
Le frequenze dei metallo carbonili sono proporzionali alla forza del legame C-O e inversamente proporzionali alla forza della retrodonazione π tra metallo e carbonio.
Sintesi
Le reazioni di sintesi dei metallo carbonili sono oggetto di ricerche continue stante la loro importanza. Si riportano solo alcune delle sintesi principali
1) Reazione diretta tra metallo e CO
Il nichel e il ferro allo stato elementare possono dare i rispettivi metallo carbonili:
Ni + 4 CO → Ni(CO)4
Fe + 5 CO → Fe(CO)5
2) Riduzione dei sali metallici e degli ossidi
Alcuni metallo carbonili vengono preparati dalla riduzione degli alogenuri metallici in presenza di monossido di carbonio ad alta pressione in presenza di agenti riducenti quali rame, alluminio e idrogeno; ad esempio si può ottenere il cromo esacarbonile a partire da cloruro di cromo (III) in benzene in presenza di alluminio quale agente riducente e di cloruro di alluminio quale catalizzatore:
CrCl3 + Al + 6 CO → Cr(CO)6 + AlCl3

