Il fluoruro di calcio è un composto inorganico avente formula CaF2 presente nel minerale fluorite. che costituisce la maggiore fonte di fluoro a livello mondiale. Alla metà dell’800, il chimico francese Henri Sainte-Claire Deville scoprì che il fluoruro di calcio poteva essere ottenuto dal carbonato di calcio
Proprietà del fluoruro di calcio
E’ un sale bianco, cristallino e, avendo un valore di Kps pari a 3.45 ∙ 10-11 ha una solubilità in acqua di 0.0160 g/L.
E’ insolubile in acetone ma è solubile in soluzioni acide per acido cloridrico, acido fluoridrico, acido nitrico, acido solforico in quanto la solubilità aumenta al diminuire del pH.
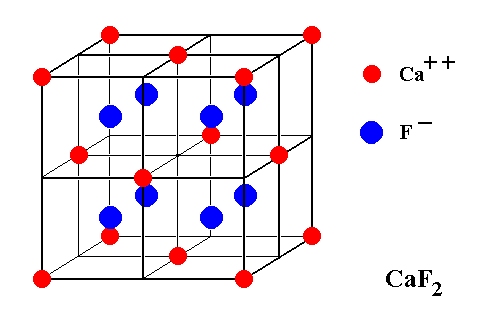
E’ un solido ionico la cui struttura è costituita da due celle cubiche semplici in cui lo ione Ca2+ coordina 8 ioni F–, mentre lo ione F– per soddisfare la regola dell’elettroneutralità locale ha numero di coordinazione 4
Sintesi
Può essere ottenuto per reazione del carbonato di calcio con acido fluoridrico con formazione di fluoruro di calcio, biossido di carbonio e acqua:
CaCO3(s) + 2 HF(aq) → CaF2(s) + CO2(g)+ H2O(l)
Ad elevate temperature reagisce con l’acido solforico concentrato per dare solfato di calcio e fluoruro di idrogeno secondo una reazione di doppio scambio:
CaF2(s) + H2SO4(aq) → CaSO4(s) + 2 HF(g)
Reazioni
Il fluoruro di calcio reagisce con l’ossido di boro per dare fluoruro di boro e ossido di calcio secondo la reazione:
3 CaF2(s) + B2O3(s) → BF3(g) + 3 CaO(s)
Il fluoruro di calcio è trasparente nella regione del visibile ma mostra assorbimento ottico nella regione dell’U.V. e dell’I.R.
Usi
È utilizzato per produrre componenti ottici come finestre e lenti, utilizzati in sistemi di imaging termico, spettroscopia e telescopi. Esso è trasparente su un’ampia gamma dalle frequenze ultraviolette (UV) a quelle infrarosse (IR). Il suo basso indice di rifrazione riduce la necessità di rivestimenti antiriflesso
Viene utilizzato nella produzione del vetro, di smalti, di agenti per saldatura e nella metallurgia dell’alluminio, per l’ottenimento di lenti speciali utilizzate nei telescopi. Esso viene utilizzato come componente ottico a causa della sua stabilità chimica in condizioni avverse. Infatti l’esposizione al 100% di umidità relativa a temperatura ambiente non appanna le superfici lucide.
Il fluoruro di calcio è comunemente usato come materiale per finestre sia per le lunghezze d’onda dell’infrarosso che dell’ultravioletto, poiché è trasparente in queste regioni (da circa 0,15 a 9 μm) e presenta un indice di rifrazione estremamente basso.
Nanoparticelle di fluoruro di calcio sono usate in alcuni dentifrici per prevenire la carie