La citocromo c ossidasi è un enzima appartenente alla classe delle ossidoreduttasi e costituisce il complesso terminale della fosforilazione ossidativa nelle cellule eucariotiche che ha luogo nei mitocondri.
La citocromo c ossidasi mitocondriale utilizza l’energia coinvolta nell’ossidazione del citocromo c e nella riduzione dell’acqua per generare un gradiente elettrochimico protonico attraverso la membrana mitocondriale interna.
Catena di trasporto degli elettroni
La catena di trasporto degli elettroni si trova nella membrana mitocondriale interna delle cellule eucariotiche e nella membrana plasmatica delle cellule procariotiche. Nelle cellule eucariotiche, i protoni sono pompati dalla matrice mitocondriale allo spazio intermembrana. Il potenziale elettrochimico generato dal gradiente protonico alimenta la generazione di ATP da parte dell’ATP sintasi, enzima appartenente alla classe delle idrolasi
Reazione
La citocromo c ossidasi riduce l’ossigeno molecolare ad acqua secondo la reazione
4 Cyt c + 4H + + O2 + 4H +(matrice) → 4 Cyt c ox + 2 H 2O + 4H+(spazio intermembrana)
La reazione richiede quattro elettroni donati dalla citocromo c e portatore di elettroni e quattro protoni che sono trasferiti dalla matrice allo spazio intermembrana. Ogni citocromo c trasporta solo un elettrone, sono necessarie quattro molecole di citocromo c.
Struttura
È un complesso dimerico costituito da 13 subunità proteiche contenente tre ioni rame e due gruppi eme detti rispettivamente eme a e eme a3.
Le tre subunità più grandi sono codificate dal DNA mitocondriale e formano un nucleo enzimatico reattivo. Queste subunità sono conservate nei procarioti e negli eucarioti e sono responsabili della maggior parte dell’attività catalitica. Le restanti 10 subunità sono codificate dal DNA
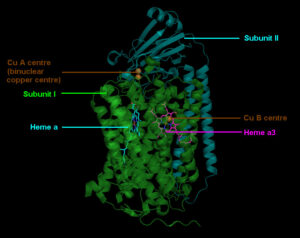 La citocromo c ossidasi ha quattro centri redox attivi che devono tutti caricarsi di elettroni per realizzare la reazione dato che per la riduzione di O2 sono necessari 4 elettroni.
La citocromo c ossidasi ha quattro centri redox attivi che devono tutti caricarsi di elettroni per realizzare la reazione dato che per la riduzione di O2 sono necessari 4 elettroni.
I quattro centri, oltre a eme a e eme a3 sono CuA e CuB
Il sito Cu A è un centro di rame binucleare complessato con gruppi -OSH di residui di cisteina.
Questo sito è il primo sito redox a ricevere elettroni donati dal citocromo c.
La donazione di un elettrone riduce il sito dalla sua forma ossidata: Cu (I) → Cu (II)
Dopo la riduzione, il sito Cu A ritorna rapidamente allo stato ossidato, rilasciando un elettrone.
All’interno della struttura, l’eme a è coordinato da due gruppi di imidazolo di istidina, mentre l’eme a3 è coordinato da un solo imidazolo di istidina.
Citocromo c ossidasi e cianuro
L’inalazione di cianuro di idrogeno o l’ingestione di un sale contenente cianuro come NaCN o KCN in dosi elevate o per un tempo prolungato porta alla morte. Lo ione CN–, infatti, blocca la catena respiratoria e quindi la respirazione cellulare con l’immediata caduta della produzione di ATP.
Esso si lega al gruppo prostetico eme presente nella citocromo c ossidasi. Gli elettroni non sono in grado di legarsi con l’ossigeno, il che impedisce ad altri elettroni di muoversi lungo la catena respiratoria. Poiché gli elettroni non sono in grado di fluire lungo la catena, i protoni non sono pompati nello spazio interno della membrana e l’ATP sintasi non ha protoni con cui sintetizzare l’ATP privando le cellule, i tessuti e, in definitiva, l’intero corpo di ossigeno.
