La cheratina è una proteina fibrosa scarsamente solubile a causa dell’elevata presenza di amminoacidi idrofobici. La cheratina è considerata il biopolimero proteico più disponibile in commercio al mondo.
Si trova principalmente nelle cellule epiteliali dei vertebrati superiori e contiene il più alto contenuto proteico Essa presenta un elevato contenuto di zolfo di cui sono costituiti i capelli, le unghie e, negli animali gli artigli, le corna, i becchi e il carapace. A causa della bassa tossicità, il biopolimero viene utilizzato in applicazioni biomediche, cosmeceutiche e industriali e trova applicazione nella cura della pelle e in altre applicazioni cosmetiche.
I progressi nell’estrazione, purificazione e caratterizzazione delle cheratine hanno portato alla crescita esponenziale dei materiali cheratinici e dei loro derivati come componenti fibrosi nei biomateriali, grazie al fatto che le proteine estratte dalla cheratina, hanno una capacità intrinseca di autoassemblarsi e polimerizzare in strutture porose e fibrose.
Ha una certa capacità intrinseca di facilitare l’adesione cellulare, la proliferazione e la rigenerazione del tessuto, pertanto i biomateriali a base di cheratina possono fornire una matrice biocompatibile per la ricrescita e la rigenerazione dei tessuti.
Una delle importanti applicazioni biomediche del polimero è nei sistemi di somministrazione di farmaci. Gli idrogel di cheratina sono utilizzati anche in varie applicazioni di ingegneria tissutale come l’ingegneria del tessuto osseo, la rigenerazione oculare, la guarigione delle ferite, la rigenerazione dei nervi e la sostituzione della pelle
Classificazione
Sulla base della struttura secondaria è classificata come:
α-cheratina costituita da α eliche destrorse intrecciate che è debolmente basica e si trova solitamente nei tessuti molli come la lana, la pelle e il vello delle pecore,
β-cheratina costituita da foglietti β che è debolmente acida e i trova nei tessuti duri come le piume degli uccelli, le corna, gli artigli e gli zoccoli
L’α-cheratina è costituita da due α eliche destrorse in un superavvolgimento sinistrorso che formano un dimero. Due dimeri di associano tra loro tramite un meccanismo testa-coda per dare i protofilamenti che a loro volta dimerizzano in protofibrille stabilizzate da ponti disolfuro. L’associazione di quattro protofilamenti danno luogo alla formazione di una microfibrilla.
Francis Crick e Linus Pauling, scoprirono che queste α-cheratine erano disposte in spire arrotolate
Struttura della cheratina
Le cheratine contengono una elevata quantità di cisteina, amminoacido caratterizzato dalla presenza del gruppo –SH. Un elevato contenuto di cisteina (7–13%) differenzia le cheratine da altre proteine strutturali, come il collagene e l’elastina. I gruppi tiolici tendono ad accoppiarsi e formano un legame covalente –S-S- a seguito di una ossidazione.
I ponti disolfuro conferiscono alla cheratina robustezza e rigidità oltre che stabilità termica; se è bruciata la cheratina emana un odore pungente dovuto alla presenza di composti solforati che si formano.

Le cheratine contengono una elevata percentuale di glicina e di alanina che sono gli amminoacidi più semplici. Nel caso della struttura a β-foglietto l’elevata percentuale di gruppi laterali semplici, idrogeno e gruppo metilico rispettivamente, consente la formazione di legami a idrogeno senza che vi sia l’impedimento tra i gruppi amminici e i gruppi carbossilici dei legami peptidici presenti su catene adiacenti.
Sono presenti inoltre legami ionici tra gruppi –NH3+ e –COO– Quando si fa la permanente viene inizialmente aggiunta una sostanza riducente basica come il tioglicolato di ammonio HS-CH2-COO–NH4+ che riduce e rompe i ponti disolfuro.
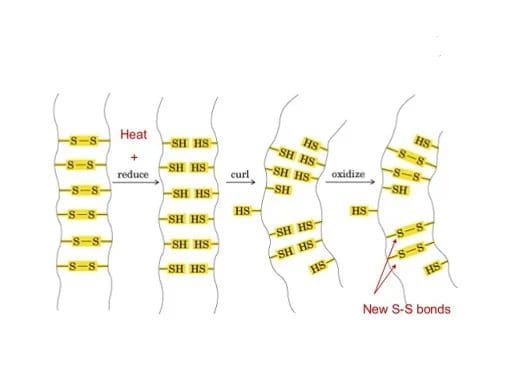
A questo punto i capelli vengono messi sui bigodini e aggiunto un agente ossidante come una soluzione diluita di perossido di idrogeno in modo che i ponti disolfuro vengano riformati nelle nuove posizioni e quindi i capelli si presenteranno ricci.
I legami disolfuro consentono alla cheratina di ottenere una struttura tridimensionale compatta con elevata resistenza alle reazioni idrolitiche chimiche o enzimatiche, contribuendo alla resilienza fisica della struttura
